L’età avanzata del padre al momento del concepimento è associata a un aumento delle mutazioni de novo nella linea germinale maschile, con implicazioni per un gruppo specifico di patologie congenite dominanti e per condizioni del neurosviluppo. Quali sono i meccanismi biologici alla base del cosiddetto “effetto dell’età paterna” e il rischio cromosomico e genetico documentati dalla letteratura scientifica dovuti all’età del padre? E qual è il ruolo del test prenatale non invasivo (NIPT) come strumento di screening nelle gravidanze con padre di età avanzata?
L’età paterna avanzata: un fenomeno in crescita
Negli ultimi decenni, l’età media alla paternità è aumentata in modo consistente nei paesi ad alto reddito. Ad esempio, secondo i dati riportati in una revisione pubblicata su ScienceDirect nel 2022, nel Regno Unito l’età media standardizzata dei padri al momento della nascita del figlio era di 33,7 anni nel 2020, il valore più alto da quando questi dati vengono sistematicamente registrati, rispetto ai 29,7 anni del 1970. Negli Stati Uniti, un’analisi storica ha documentato un aumento dell’età paterna media da 27,4 anni nel 1972 a 30,9 anni nel 2015.
In Italia il fenomeno assume proporzioni ancora più marcate. Secondo i dati ISTAT ripresi di recente dal Sole 24 Ore, l’età media alla nascita del primo figlio per gli uomini si attesta oggi a 35,8 anni, il valore più alto registrato in Europa davanti a Francia (33,9 anni) e Germania (33,2). Si tratta di un incremento di circa dieci anni rispetto alla fine degli anni Novanta, quando il primo figlio arrivava mediamente intorno ai 25 anni, una traiettoria più rapida e accentuata di quella osservata nei Paesi anglosassoni. Oggi un uomo su tre in Italia non ha ancora avuto figli dopo i 36 anni, e nel 2021 oltre il 10% dei parti ha riguardato coppie con almeno un genitore di età superiore ai 40 anni.
Questo spostamento demografico non è privo di conseguenze biologiche. A differenza dell’effetto dell’età materna, ampiamente studiato e comunicato in ambito ostetrico, l’impatto dell’età del padre e del rischio genetico, quindi della salute riproduttiva e genetica della prole, ha ricevuto storicamente meno attenzione clinica, pur essendo supportato da un corpo crescente di evidenze scientifiche. Storicamente, società come la American Society for Reproductive Medicine, la British Andrology Society e la Canadian Fertility and Andrology Society avevano adottato il limite di 40 anni come soglia raccomandabile per i donatori di sperma. Tale soglia è tuttora in vigore nelle linee guida ASRM, mentre le linee guida britanniche aggiornate nel 2019 l’hanno innalzata a 45 anni sulla base di nuove evidenze.
Età del padre e rischio genetico per il feto: perché la spermatogenesi è diversa dall’oogenesi
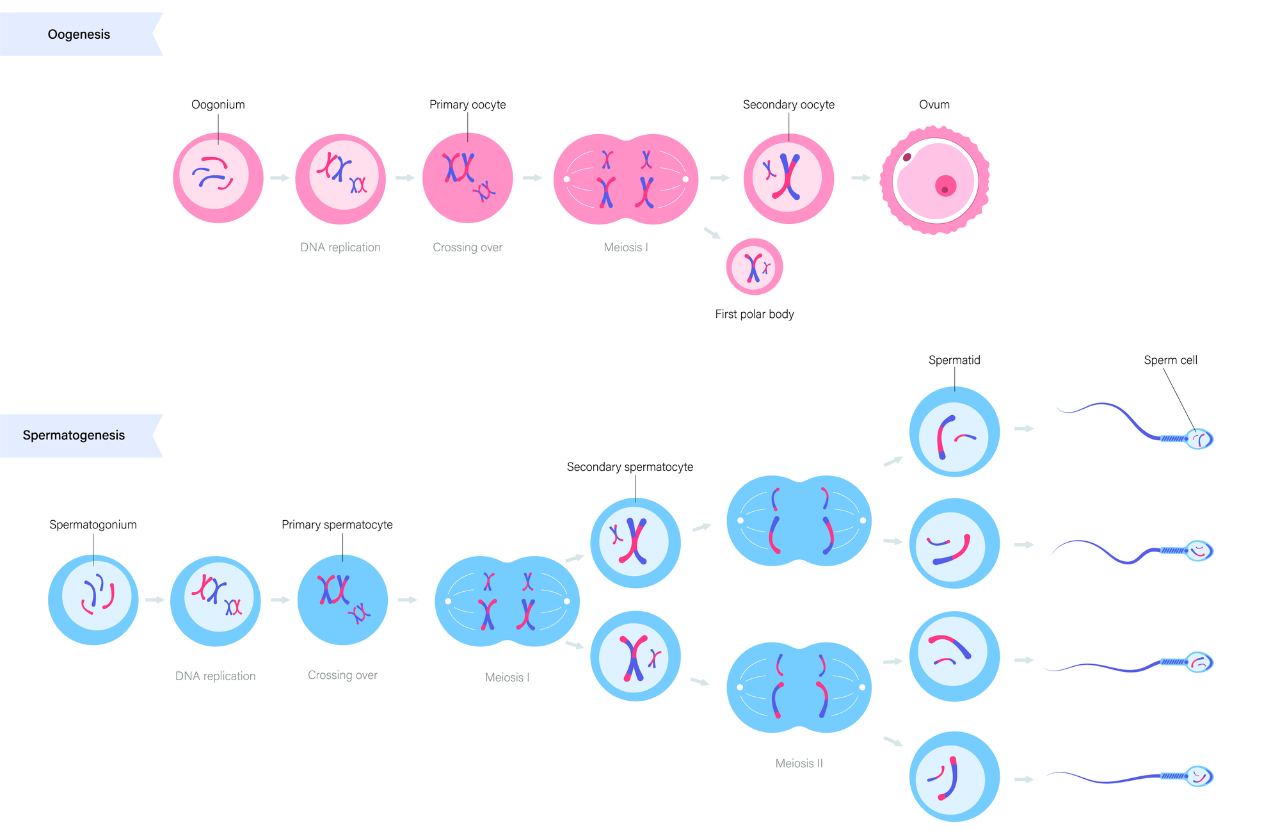
Per comprendere il rischio genetico legato all’età del padre è necessario partire da una differenza fondamentale nella biologia riproduttiva dei due sessi. Le cellule uovo femminili completano la maggior parte delle loro divisioni cellulari durante la vita fetale e rimangono poi in uno stato di quiescenza fino all’ovulazione: questo le rende vulnerabili soprattutto agli errori meiotici di non disgiunzione cromosomica, come quelli che portano alla trisomia 21, un rischio che aumenta con l’età materna.
La spermatogenesi maschile funziona in modo radicalmente diverso. Le cellule staminali spermatogoniali si dividono in modo continuo per tutta la vita riproduttiva dell’uomo, con circa 23 divisioni per anno. Va precisato che questo valore è un’approssimazione poiché stime classiche suggeriscono anzi un tasso in lieve decrescita con l’età, e analisi recenti su sperma con tecnologia NanoSeq (2025) mostrano un accumulo mutazionale lineare (~1,67 mutazioni/anno per genoma aploide) non perfettamente sovrapponibile al modello esponenziale di Kong, un tema ancora oggetto di discussione scientifica.
Come riscontrabile dalla documentazione scientifica, è stimabile che gli spermatozoi prodotti da un uomo di 25 anni abbiano subito circa 350 divisioni cellulari, mentre quelli di un uomo di 45 anni derivino da cellule che hanno attraversato circa 750 replicazioni. Ogni replicazione del genoma introduce una probabilità di errori di copia, e questi errori si accumulano progressivamente nel tempo.
Secondo i dati di studi di sequenziamento dell’intero genoma su trii genitore-figlio, circa il 75-80% delle mutazioni de novo (DNM) rilevate nei neonati ha origine paterna. Questa proporzione riflette direttamente la differenza quantitativa nelle divisioni cellulari tra le due linee germinali. Una ricerca seminale pubblicata su Nature da Kong et al. 2012 e poi confermata da studi su larga scala ha mostrato che il numero di mutazioni de novo di origine paterna aumenta a una velocità di circa 4,28% per anno, con un raddoppio ogni 16,5 anni circa e un aumento stimato di 8 volte nell’arco di 50 anni di età paterna.
Mutazioni de novo e rischio numerico: la distinzione tra aneuploidie e varianti puntiformi
Un aspetto cruciale per la comprensione del rischio genetico associato all’età del padre è la distinzione tra due categorie di alterazioni cromosomiche e genetiche: le aneuploidie (alterazioni nel numero dei cromosomi) e le mutazioni de novo puntiformi o strutturali a carico di singoli geni.
Le aneuploidie fetali, come la trisomia 21 (sindrome di Down), la trisomia 18 (sindrome di Edwards) e la trisomia 13 (sindrome di Patau), derivano prevalentemente da errori nella meiosi materna e il loro rischio aumenta in modo documentato con l’avanzare dell’età della madre. Il contributo paterno alle aneuploidie autosomiche standard è considerato marginale, sebbene non del tutto assente: tutti gli uomini producono una percentuale di spermatozoi aneuplodi compresa tra il 3 e il 5%, e alcuni studi hanno suggerito che gli eventi di non disgiunzione a carico dei cromosomi sessuali aumentino con l’età paterna.
La ricerca pubblicata su Frontiers in Endocrinology da Chan e Robaire (2022) riporta che le anomalie cromosomiche strutturali de novo hanno un’origine prevalentemente paterna. In continuità con quanto documentato da Thomas et al. (2006), circa il 70% delle delezioni terminali, l’84% delle delezioni interstiziali e anomalie ad anello, il 58% delle piccole duplicazioni e il 62% delle traslocazioni sbilanciate risultano di origine paterna, per un’aggregata stimabile intorno al 72% dei riarrangiamenti non bilanciati.
Le mutazioni de novo puntiformi (dnSNV, de novo single nucleotide variants) rappresentano la categoria di varianti più direttamente collegata all’invecchiamento spermatogoniale. Come evidenziato da uno studio pubblicato su Nature Communications da Taylor e colleghi (2019) e basato su dati di sequenziamento dell’esoma su trii genitore-figlio, queste varianti conferiscono un contributo reale, anche se moderato, al rischio di disturbi del neurosviluppo come il disturbo dello spettro autistico, la schizofrenia, la disabilità intellettiva, l’epilessia e le cardiopatie congenite. Gli autori sottolineano che, per i disturbi più complessi come autismo e schizofrenia, il rischio epidemiologico osservato nei figli di padri anziani riflette probabilmente una combinazione di fattori, non tutti direttamente correlati all’età.
Età del padre e rischio genetico per il feto: la “selezione spermatogoniale egoista”
Esiste una categoria distinta e meglio caratterizzata di condizioni genetiche per cui il legame con l’età paterna è particolarmente forte, i cosiddetti disturbi da effetto età paterna (PAE disorders, Paternal Age Effect disorders). Si tratta di un gruppo ristretto di patologie autosomiche dominanti causate da mutazioni de novo puntiformi specifiche, che presentano tre caratteristiche inusuali: origine quasi esclusivamente paterna, forte associazione con l’età avanzata del padre al concepimento e una frequenza di mutazione germinale molto superiore alla media genomica.
I principali disturbi PAE comprendono la sindrome di Apert (mutazioni di FGFR2), l’acondroplasia e la displasia tanatofora (mutazioni di FGFR3), la sindrome di Costello (HRAS), la sindrome di Noonan (PTPN11), la sindrome di Crouzon, la sindrome di Pfeiffer, la sindrome di Muenke, e le neoplasie endocrine multiple di tipo 2A e 2B (RET). Questi nove disturbi corrispondono a mutazioni puntiformi specifiche in soli cinque geni. La frequenza di mutazione osservata per alcune di queste varianti è fino a 1.000 volte superiore alla frequenza media di background del genoma umano, un dato di per sé anomalo che ha stimolato ricerche approfondite sui meccanismi sottostanti.
Il meccanismo proposto e oggi ampiamente accettato è la cosiddetta “selezione spermatogoniale egoista” (selfish spermatogonial selection). Secondo questo modello, alcune mutazioni nei geni della via di segnalazione RTK/RAS (che regola la proliferazione e la sopravvivenza cellulare) conferiscono un vantaggio selettivo alle cellule staminali spermatogoniali che le portano: queste cellule si dividono più rapidamente delle cellule sane circostanti, espandendosi clonalmente all’interno del testicolo e producendo nel tempo una proporzione crescente di spermatozoi portatori della mutazione. Il processo è stato paragonato a una forma localizzata di oncogenesi benigna nel tessuto testicolare.
L’analogia con la biologia tumorale non è casuale: le stesse mutazioni nei geni FGFR2, FGFR3, HRAS e RET che nella linea germinale causano i disturbi PAE sono frequentemente riscontrate nei tumori somatici. La differenza è che nel contesto spermatogoniale la cellula mutata non forma un tumore, ma produce cloni di spermatozoi che trasmettono la mutazione alla prole. Studi di dissecazione testicolare su campioni cadaverici hanno confermato la presenza di cluster localizzati di cellule mutanti in testi normali di uomini adulti, con una distribuzione spaziale eterogenea che rispecchia il modello di espansione clonale.
La conseguenza pratica è che il rischio genetico dell’età del padre, quindi di trasmettere queste mutazioni, non cresce linearmente con l’età, ma in modo esponenziale: padri di 50 anni o più hanno un rischio di avere figli con acondroplasia circa 10 volte superiore rispetto a padri più giovani. Per la sindrome di Apert, il rischio relativo per padri oltre i 50 anni è stimato in circa 9,5 volte rispetto ai padri sotto i 29 anni, secondo i dati riportati su Andrology da Gourinat e colleghi (2023).
Età del padre e rischio genetico per il feto: autismo e schizofrenia
Accanto ai disturbi PAE strutturalmente ben definiti, la letteratura scientifica ha documentato un’associazione robusta tra età paterna avanzata e rischio aumentato di disturbi del neurosviluppo, in particolare il disturbo dello spettro autistico (ASD) e la schizofrenia. Uno studio di coorte basato sulla popolazione condotto in Svezia su circa 750.000 individui nati tra il 1973 e il 1980 (Sipos et al., BMJ 2004) ha confermato questa associazione, con una particolarità rilevante: il legame tra età paterna e schizofrenia era evidente soprattutto nei casi senza storia familiare del disturbo, suggerendo che le mutazioni de novo nella linea germinale paterna possano costituire un fattore causale indipendente.
Una meta-analisi dose-risposta pubblicata su Acta Psychiatrica Scandinavica da Wu e colleghi (2017), basata su 27 studi epidemiologici, ha mostrato che a ogni incremento di 10 anni nell’età del padre corrisponde un aumento del 21% del rischio di autismo nella prole. Questi risultati sono stati ulteriormente confermati da un grande studio di coorte multinazionale pubblicato su Molecular Psychiatry (Sandin et al., 2016), che su oltre 5,7 milioni di bambini nati in cinque paesi ha documentato un rischio di autismo superiore del 66% nei figli di padri di 50 anni o più rispetto ai figli di padri di 20-29 anni. Ulteriori analisi hanno indicato che i figli di padri con più di 35 anni presentano un rischio circa 2,1 volte superiore di sviluppare sintomi psicotici rispetto ai figli di padri più giovani, mentre l’età materna non mostrava lo stesso effetto.
Tuttavia, la natura di questa associazione è oggetto di dibattito attivo nella comunità scientifica. Lo studio di Taylor e colleghi su Nature Communications (2019) ha precisato che le varianti de novo puntiformi di origine paterna spiegano solo una quota limitata del rischio epidemiologico osservato per autismo e schizofrenia nei figli di padri anziani: altri fattori, come varianti genetiche ereditarie che influenzano sia la tempistica della riproduzione che il rischio del disturbo nella prole, o fattori ambientali ed epigenetici, contribuiscono in modo significativo all’associazione osservata. Il rischio individuale per ogni singola gravidanza rimane basso in termini assoluti, anche se l’impatto a livello di salute pubblica, dato il progressivo aumento dell’età paterna media, non è trascurabile.
Modificazioni epigenetiche e altri meccanismi

Oltre alle mutazioni puntiformi e alle alterazioni cromosomiche strutturali, l’età paterna avanzata è associata ad alterazioni della regolazione epigenetica del genoma spermatico. Con l’invecchiamento si osservano modificazioni nei pattern di metilazione del DNA e nella struttura della cromatina degli spermatozoi, con potenziali conseguenze sullo sviluppo embrionale precoce. Alcuni studi hanno ipotizzato che queste modificazioni possano aumentare il rischio di alcune rare patologie epigenetiche nella prole concepita con tecnologie di riproduzione assistita (ART), sebbene i dati rimangano ancora preliminari su questo specifico aspetto.
Si aggiungono anche l’aumento dello stress ossidativo a carico del DNA spermatico con l’avanzare dell’età, la riduzione dell’efficienza dei meccanismi di riparazione del DNA nelle cellule germinali anziane, e un incremento della frammentazione del DNA spermatico. Questi fenomeni contribuiscono sia alla riduzione della fertilità che all’aumento del rischio di aborto spontaneo.
Età del padre e rischio genetico per il feto: quando si parla di “età paterna avanzata”
La definizione di “età paterna avanzata” (Advanced Paternal Age, APA) non è universalmente standardizzata nella letteratura clinica. La soglia di 40 anni è quella più frequentemente adottata negli studi scientifici e nelle raccomandazioni delle società specialistiche, in particolare per quanto riguarda i donatori di sperma. Alcune pubblicazioni utilizzano 35 anni come soglia per analisi epidemiologiche, mentre altre considerano 45 o 50 anni come soglie di rischio più elevato, in particolare per i disturbi PAE come l’acondroplasia. Secondo i dati di Frontiers in Endocrinology, circa lo 0,33% dei neonati nasce con un’alterazione numerica dei cromosomi, derivante prevalentemente dalla linea germinale materna, ma il contributo paterno alle alterazioni strutturali de novo è quantitativamente rilevante.
È importante sottolineare che il rischio assoluto per ogni singola gravidanza rimane basso anche in presenza di età paterna avanzata: la revisione di Wood e Goriely (2022) pubblicata su Fertility and Sterility sintetizza la letteratura concludendo che il rischio individuale di malattia nella prole attribuibile all’età paterna avanzata rimane piccolo, ma l’impatto complessivo sulla salute pubblica non è trascurabile, soprattutto considerando il continuo aumento dell’età media dei padri al concepimento. Il rischio non giustifica posizioni allarmistiche, ma sostiene la pertinenza di uno screening prenatale informato, in particolare nei casi in cui l’età paterna sia uno dei fattori di rischio presenti.
Il NIPT nelle gravidanze con padre di età avanzata
Il test prenatale non invasivo (NIPT), basato sull’analisi del DNA libero fetale circolante nel plasma materno, è oggi il metodo di screening più sensibile e specifico disponibile per le aneuploidie cromosomiche fetali più comuni. Le linee guida dell’American College of Obstetricians and Gynecologists (ACOG) raccomandano che il NIPT sia discusso e offerto a tutte le pazienti in gravidanza, indipendentemente dall’età o dal profilo di rischio, proprio in ragione dell’elevata performance diagnostica per trisomia 21, 18 e 13.
Per quanto riguarda il rischio specifico correlato all’età paterna, il NIPT standard ha però una copertura limitata. Il NIPT classico è progettato per rilevare alterazioni nel numero di cromosomi interi o di grandi segmenti cromosomici, non le mutazioni puntiformi de novo nei singoli geni che caratterizzano i disturbi PAE. Il rilevamento di aneuploidie sessuali, su cui l’età paterna potrebbe avere un ruolo, è incluso nei pannelli NIPT estesi.
Negli ultimi anni si è sviluppata una nuova frontiera dello screening prenatale, cioè, il NIPT per malattie a singolo gene (NIPT-SGD), che utilizza il sequenziamento di nuova generazione per rilevare varianti patogene de novo o ereditate dal padre in un pannello di geni associati a patologie dominanti. Uno studio clinico condotto su 2.208 gravidanze, ha valutato le prestazioni di un pannello NIPT-SGD che copriva 25 condizioni dominanti, tra cui lo spettro delle sindromi di Noonan, le sindromi da craniosinostosi, la sindrome di Cornelia de Lange e la sindrome CHARGE. Il 5,7% delle donne ha ricevuto un risultato positivo. I tassi più elevati di positività si osservavano in presenza di anomalie ecografiche fetali o storia familiare, mentre per la sola età paterna avanzata (≥40 anni) come unico fattore di rischio, il tasso di positività era dello 0,2%, pari a 2 casi su 912.
Questa evidenza indica che il NIPT-SGD ha la sua utilità maggiore quando l’età paterna avanzata si associa ad altri indicatori clinici, come anomalie ecografiche delle ossa lunghe fetali (con un tasso di positività del 33,7% nel citato studio), anomalie craniofacciali (28,6%) o malformazioni cardiache maggiori (12,9%). L’esperto Peter Benn, dell’Università del Connecticut, ha commentato i risultati sottolineando che l’incidenza delle varianti de novo autosomiche è ritenuta superiore nelle gravidanze con padri più anziani e che “questo test potrebbe essere più fortemente indicato per i padri più anziani”.
Sul fronte tecnologico, la ricerca ha sviluppato metodi che permettono di combinare in un unico test lo screening delle aneuploidie cromosomiche standard e la rilevazione di mutazioni de novo in geni specifici, come dimostrato da uno studio pubblicato su Prenatal Diagnosis da Yang e colleghi (2021) con il metodo TAGs-seq, capace di rilevare simultaneamente aneuploidie fetali, mutazioni de novo di FGFR3 (acondroplasia, displasia tanatofora) e varianti di HBB di origine paterna correlate alla beta-talassemia.
Limiti del NIPT e ruolo della diagnostica invasiva

È fondamentale che le coppie ricevano un’informazione accurata sui limiti del NIPT, indipendentemente dall’età paterna. Il NIPT è un test di screening, non diagnostico e questo vuol dire che un risultato negativo non esclude con certezza tutte le alterazioni genetiche possibili, e un risultato positivo dovrebbe essere confermato tramite diagnostica invasiva (villocentesi o amniocentesi) prima di assumere decisioni cliniche.
Il NIPT standard non è in grado di rilevare le mutazioni puntiformi responsabili dei disturbi PAE nella loro forma de novo, a meno che non venga eseguito un pannello NIPT-SGD specifico. Allo stesso modo, molte condizioni genetiche rare non sono rilevabili con nessuna forma di NIPT attualmente disponibile, e la diagnostica prenatale completa attraverso villocentesi o amniocentesi con array-CGH o sequenziamento dell’esoma fetale rimane il gold standard per le coppie che desiderano la massima informazione genetica disponibile.
Un approccio integrato che combina l’ecografia del primo trimestre con la misurazione della translucenza nucale e il NIPT rappresenta la strategia ottimale nel primo trimestre. In presenza di anomalie strutturali ecografiche o di fattori di rischio specifici, la diagnostica invasiva con microarray cromosomico rimane la scelta raccomandata.
Counseling prenatale e comunicazione del rischio
Uno degli aspetti più delicati nella gestione delle gravidanze con padre di età avanzata è la comunicazione del rischio in modo accurato e non allarmante. I dati scientifici mostrano un aumento relativo del rischio per alcune condizioni specifiche, ma i rischi assoluti per ogni singola gravidanza rimangono bassi nella grande maggioranza dei casi. Un approccio informato al counseling genetico prenatale prevede che le coppie comprendano la differenza tra rischio relativo e rischio assoluto, la distinzione tra i tipi di alterazioni genetiche potenzialmente correlate all’età paterna, e le possibilità di screening disponibili.
È raccomanda una consulenza genetica completa per le coppie con età paterna avanzata, con discussione delle opzioni disponibili: NIPT standard per le aneuploidie, valutazione ecografica morfologica al secondo trimestre, eventuale NIPT-SGD nei casi con fattori di rischio aggiuntivi, e offerta della diagnostica invasiva per le coppie che desiderano informazioni più complete. La consulenza genetica è una componente irrinunciabile di questo percorso, non sostituibile dalla sola richiesta del test.
Il Prenatalsafe® e lo screening prenatale non invasivo

PrenatalSafe®, sviluppato da Eurofins Genoma, è un test prenatale non invasivo che analizza il DNA fetale libero circolante nel sangue materno. Eseguibile a partire dalla decima settimana di gravidanza con un semplice prelievo ematico, utilizza tecnologie di sequenziamento di nuova generazione per rilevare le principali anomalie cromosomiche del feto.
È disponibile in nove livelli di approfondimento, che permettono di adattare l’esame al quadro clinico della singola gravidanza, dalla rilevazione delle trisomie 21, 18 e 13 (PrenatalSafe® 3) fino all’analisi completa del cariotipo fetale e delle principali sindromi da microdelezione (PrenatalSafe® Karyo Plus), con una sensibilità superiore al 99% per la trisomia 21. Per le coppie con padre di età avanzata, il test permette di valutare con elevata accuratezza il rischio di aneuploidie cromosomiche (comprese quelle dei cromosomi sessuali, su cui l’età paterna può avere un ruolo) senza i rischi associati alle tecniche invasive.
GeneSafe®: il NIPT per le malattie a singolo gene correlate all’età paterna
Per le mutazioni puntiformi de novo nei singoli geni, cioè, quelle responsabili dei disturbi più strettamente legati all’età paterna avanzata, il NIPT convenzionale non è sufficiente. È per rispondere a questa esigenza che Eurofins Genoma ha sviluppato GeneSafe®, un test di screening prenatale non invasivo che analizza il DNA fetale libero alla ricerca di varianti patogene in un pannello di geni associati a patologie dominanti.
GeneSafe® è disponibile in tre livelli:
- GeneSafe® Inherited, focalizzato sulle malattie genetiche a trasmissione ereditaria (fibrosi cistica, beta-talassemia, anemia falciforme, sordità ereditaria)
- GeneSafe® De novo, dedicato alle mutazioni che insorgono spontaneamente durante la formazione dell’embrione, la cui incidenza è correlata all’età paterna avanzata. Il pannello copre 25 geni per 44 condizioni monogeniche, tra cui lo spettro delle sindromi di Noonan e delle altre RASopatie (PTPN11, RAF1, KRAS, SOS1, BRAF, NRAS e altri), le sindromi da craniosinostosi (FGFR2, FGFR3), l’acondroplasia e l’ipocondroplasia (FGFR3), la sindrome di Cornelia de Lange (NIPBL, HDAC8), la sindrome CHARGE (CHD7), la sindrome di Sotos (NSD1) e la sindrome di Alagille (JAG1).
- GeneSafe® Complete, che combina i due livelli precedenti per uno screening esteso sia delle forme ereditarie sia di quelle de novo.
Per le coppie in cui il padre ha un’età superiore ai 40 anni, GeneSafe® De novo (o Complete) rappresenta l’opzione di screening specificamente pensata per affrontare il profilo di rischio legato alle mutazioni spontanee nei singoli geni, un ambito che il NIPT cromosomico standard non copre.
Il percorso integrato PrenatalSafe® + GeneSafe®
Per chi desidera il livello massimo di informazione in un unico percorso non invasivo, è possibile scegliere versioni combinate che uniscono l’analisi cromosomica di PrenatalSafe® Karyo allo screening multigenico di GeneSafe® Complete:
- PrenatalSafe® Complete: cariotipo fetale + malattie genetiche ereditarie + de novo
- PrenatalSafe® Complete Plus: aggiunge lo studio di nove tra le più comuni sindromi da microdelezione
- PrenatalSafe® Full Risk: integra anche un carrier screening per entrambi i genitori (GeneScreen® Focus)
La scelta della versione più appropriata va sempre discussa con il medico specialista in genetica, tenendo conto dell’età materna e paterna, dell’eventuale presenza di anomalie ecografiche, della storia familiare e del quadro clinico complessivo. Un risultato positivo al NIPT, che si tratti di aneuploidie o di mutazioni monogeniche, è un dato di screening che dovrebbe essere confermato tramite diagnostica invasiva (villocentesi o amniocentesi) prima di qualunque decisione clinica, all’interno di un percorso di consulenza genetica strutturata.

